Trends Cell Biol | 吕志民团队全面总结糖代谢酶对基因表达的调控
细胞代谢与基因转录是生物体内相互调节的两个基本生物学过程。肿瘤细胞中,葡萄糖代谢(糖酵解和糖异生)相关基因的异常表达,可促进有氧糖酵解的发生。更为重要的是,参与糖酵解或糖异生的酶还具有代谢功能之外的非经典功能,可通过调节染色质或转录复合物重塑,直接调控肿瘤基因的表达,从而促进肿瘤发生发展。细胞代谢与基因表达这一相互调节网络是肿瘤细胞的独有特征,为癌症治疗提供了独特的功能靶点和治疗策略。
2022年3月15日,浙江大学转化医学研究院吕志民教授团队在Trends in Cell Biology在线发表了题为Regulation of gene expression by glycolytic and gluconeogenic enzymes的综述,全面总结了糖酵解及糖异生通路中代谢酶在基因表达调控中的重要功能及最新研究进展,并针对这些代谢酶的非经典功能提出了肿瘤干预治疗的新策略。这是继2018年的Regulation of chromatin and gene expression by metabolic enzymes and metabolites(Nat Rev Mol Cell Bio| 表观遗传学与代谢的交叉)、Metabolic Kinases Moonlighting as Protein Kinases(Trends in Biochemical Sciences.)、2020年的Lipid metabolism and cancer(JEM综述 | 吕志民等揭示脂质代谢与肿瘤发生发展的相互关系)以及2021年的The evolving landscape of noncanonical functions of metabolic enzymes in cancer and other pathologies (Cell Metab综述 | 吕志民团队总结代谢酶在癌症等疾病发生发展中的非经典功能)四篇综述之后,吕志民教授团队对肿瘤代谢新认知的又一全面总结。

糖酵解是葡萄糖的分解代谢过程,以产生能量以及生物大分子合成所需的原料。在肿瘤细胞中,糖酵解所产生的终产物丙酮酸即使在有氧条件下仍不进入三羧酸循环,而是在乳酸脱氢酶作用下产生大量乳酸。肿瘤细胞这一代谢方式的改变被称为瓦博格效应(Warburg Effect)。糖异生是糖酵解的逆向过程,由丙酮酸等三碳化合物合成葡萄糖。糖酵解和糖异生共享多个代谢酶及中间产物(图1)。近年研究发现,多数糖酵解和糖异生酶具有非代谢功能,并且能够直接参与肿瘤细胞基因表达的调控。
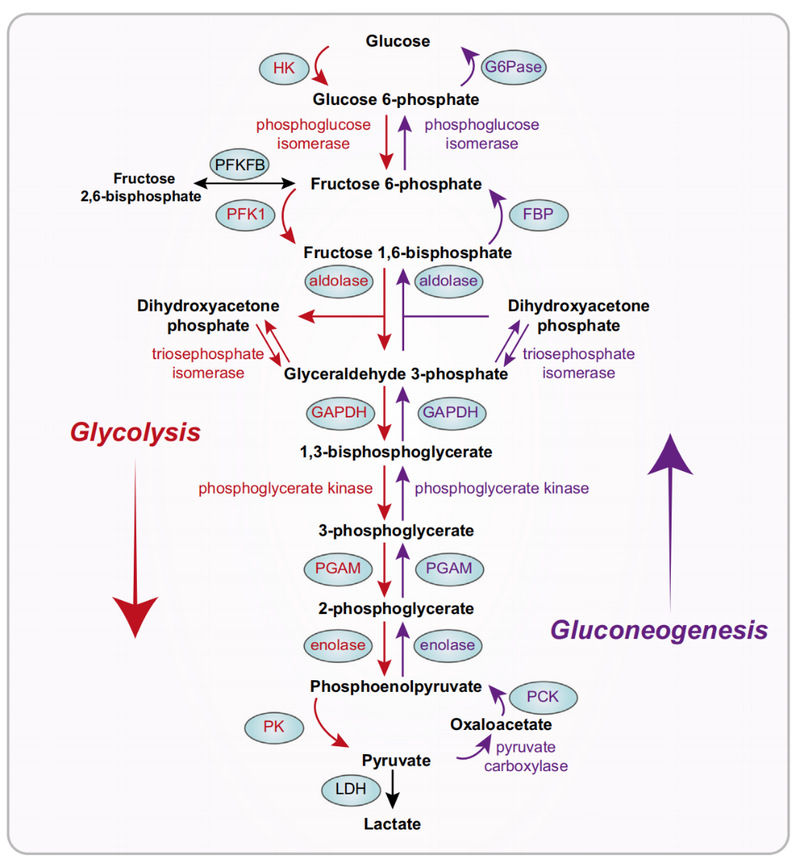
图1.糖酵解和糖异生通路中具有基因表达调控功能的代谢酶示意图。
这些酶包括(1)在糖酵解途径和乳酸产生中发挥功能的己糖激酶 (HK)、磷酸果糖激酶1 (PFK1)、6-磷酸果糖激酶-2/果糖双磷酸酶-2 (PFKFB)、丙酮酸激酶 (PK) 及乳酸脱氢酶 (LDH);(2)糖异生途径中的限速酶果糖-1,6-二磷酸酶 (FBP) 以及磷酸烯醇丙酮酸羧化激酶1 (PCK1);(3)催化糖酵解和糖异生可逆反应的醛缩酶 (aldolase)、甘油醛-3-磷酸脱氢酶 (GAPDH)、磷酸甘油变位酶 (PGAM)、烯醇酶 (enolase)。
肿瘤细胞糖酵解及糖异生通路中代谢酶直接调控基因表达的发现,为肿瘤干预治疗提供了新视角:1、阻断代谢酶核转位的信号通路;2、设计特异性靶向细胞核代谢酶的抑制剂;3、阻断细胞核内代谢酶与转录复合物的结合;4、特异性抑制代谢酶的蛋白激酶活性而不影响其代谢酶活性(图2)。
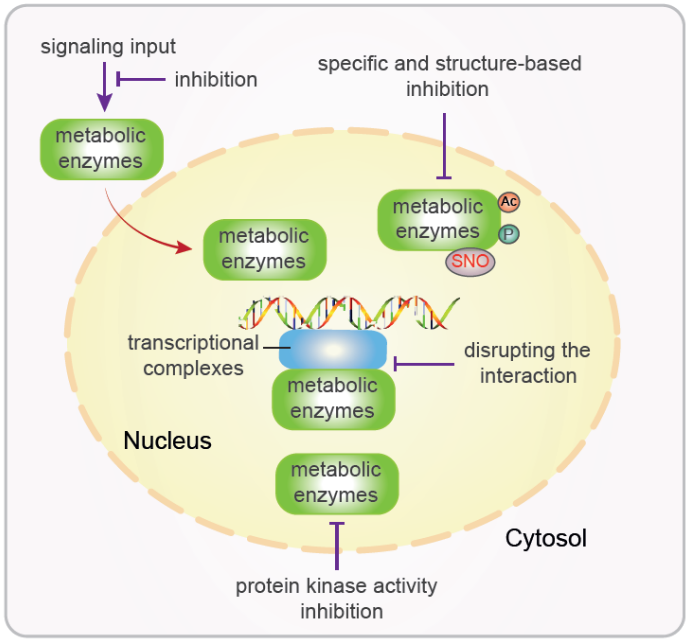
图2. 通过抑制代谢酶非经典功能治疗人类疾病的策略
吕志民教授团队在肿瘤代谢酶领域取得了许多开创性的研究成果,已发现多个代谢酶具有蛋白激酶活性(包括代谢酶PKM2、PGK1、KHK-A、PCK1、CHKα2),同时也揭示了若干其他代谢酶和代谢物在肿瘤细胞调控中具有重要的非代谢功能,极大的丰富了业界对肿瘤代谢的认知,对靶向肿瘤代谢的药物研发具有重要的指导意义。


